検査
正確な結果を早く提供することで、疑念を最小限に抑え、医療従事者と患者の皆様の意思決定および診断における自信を高めることが当社の目標です。

臨床検査
多岐に渡るアッセイメニューがあり、さらに多くのアッセイが開発中です。
細胞診
子宮頸部疾患予防の変革をリードしています。
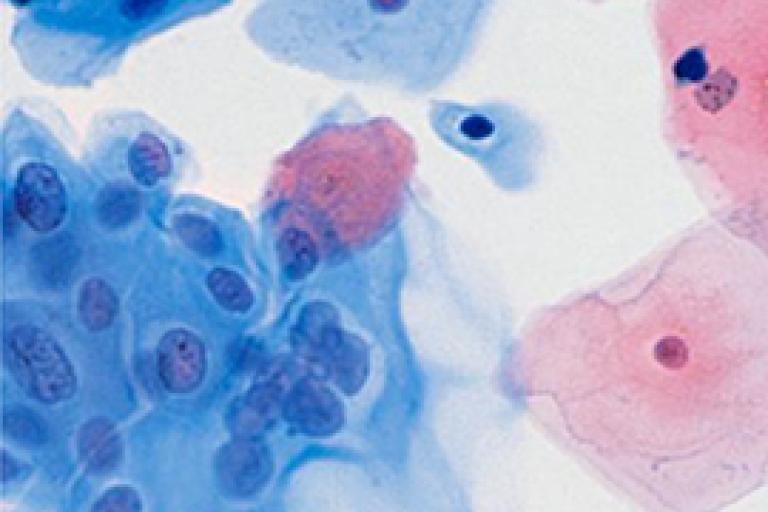
スクリーニング検査
検出力を高め、ワークフローが合理化します。
遺伝子検査
今日および将来のニーズを満たす自動化された装置と検査メニュー。

コレクションデバイス
正確で信頼性の高い結果を得るために厳密に開発されています。